INMUNOTERAPIA ESPECÍFICA
CON EXTRACTO MODIFICADO DE Salsola Kali: EFICACIA Y SEGURIDAD.
Monzón S, Venturini
M, Colás C, Lezaun A, Casanovas M*, Reichelt C, Lara S.
Hospital Clínico
Universitario. Zaragoza.
*Departamento médico.
C.B.F. Leti S.A.
INTRODUCCIÓN
El polen de la Quenopodiales (7) constituye el 5% de los pólenes anuales en el área de Zaragoza, pero sensibilizan hasta el 42% de los polínicos en nuestra área, ocupando el tercer lugar entre la población polínica de nuestra región por su gran poder sensibilizante. Debido a la gran repercusión de la misma sobre nuestros pacientes, la alta prevalencia de sensibilizaciones y a la falta de estudios sobre inmunoterapia con extracto de Salsola kali, nos planteamos diseñar un ensayo de inmunoterapia doble ciego controlado con placebo.
OBJETIVOS Y RESULTADOS PRELIMINARES
El objetivo del ensayo clínico doble-ciego, controlado con placebo, empleando un extracto despigmentado, polimerizado y adsorbido en hidróxido de aluminio, de Salsola kali, ha sido valorar tanto la eficacia como la seguridad de esta nueva inmunoterapia. Se presentan resultados preliminares del mismo.
Para apoyar la eficacia de la inmunoterapia, se ha tenido en cuenta tanto la sintomatología clínica, que es la variable principal del estudio, como los parámetros clínicos secundarios:
· Variable clínica principal: Sintomatología Clínica
o Recuento de puntuación global de síntomas
o Correlación nivel de polen de quenopodiales-Síntomas
· Parámetros Clínicos Secundarios:
o Recuento de puntuación de consumo de medicación
o Cuestionario de calidad de vida en rinitis
Para apoyar la seguridad de la inmunoterapia, aportaremos los datos de la
monitorización y tolerancia de la misma.
MÉTODOS ESTADÍSTICOS
Para el análisis estadístico de los datos se ha utilizado, en la estadística comparativa, el test de la t de Student, siendo para datos pareados en estudios intragrupo y no pareados en estudios intergrupo; para comprobar la asociación entre el contenido medioambiental de polen y el escore de síntomas se ha empleado un estudio de correlación, estudiando si la estimación del cociente de correlación obtenido es distinto de cero, mediante el test de correlación cero (“Correlation Z test”).
CUMPLIMIENTO DEL PROTOCOLO
La planificación inicial del estudio fue de 66 pacientes en total, 44 en el grupo activo y 22 en el grupo control, pero debido al retraso de un año en la aprobación del ensayo, se partió de 63 pacientes, 43 activos y 20 controles por abandono de 3 pacientes en este periodo de tiempo. A lo largo del ensayo fueron retirados 2 pacientes, uno de cada grupo, ya que no realizaban un buen cumplimiento del protocolo. Otro paciente abandonó por enfermedad grave familiar, perteneciendo al grupo activo, por lo que finalmente la muestra ha sido de un total de 60 pacientes, 41 activos y 19 controles.
CARACTERÍSTICAS DE LOS PACIENTES
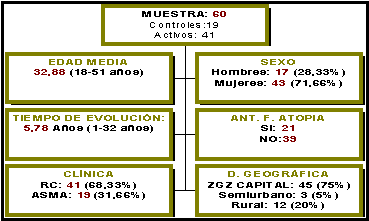
Las
características de los pacientes quedan recogidas en la siguiente tabla:
SINTOMATOLOGÍA CLÍNICA
![]()

 1.-Correlación
niveles de polen de quenopodiales-Síntomas.
1.-Correlación
niveles de polen de quenopodiales-Síntomas.
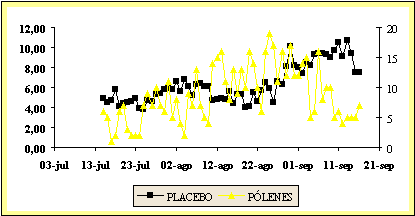
La época de
máxima polinización de Salsola kali
en la provincia de Zaragoza abarca desde mediados de Julio hasta mediados de
Septiembre. Analizando los niveles de polen medioambiental y tomando como valor
de referencia 10 granos/m3 (límite observado por
la Dra Belén de la Hoz como reactivo en su Tesis Doctoral), vemos que no existe
coincidencia en el tiempo entre el pico de máxima polinización y los días con
mayor sintomatología en el grupo placebo, por lo que realizamos un estudio de
correlación estadística entre el escore de síntomas de ambos grupos y el
contenido de polen, siendo claramente significativo con p<0,001 cuando
existía un desfase entre ambos de entre 10 y 25 días.
2.-Recuento de puntuación de síntomas.
El seguimiento de los pacientes ha demostrado que desde mediados de Julio hasta finales de Agosto muchos se encontraban fuera del área de influencia del polen de Salsola kali, ya que estaban de vacaciones. La época en que todos los pacientes estuvieron presentes fue a partir del 1 de Septiembre. Por esto, los niveles de polen atmosféricos, y lo explicado anteriormente, como periodo de estudio de sintomatología clínica se han analizado dos tiempos: 1-15 Septiembre y 15 Agosto hasta 15 Septiembre
2.1- Desde15 Agosto-15 Septiembre
Analizando la puntuación global de síntomas, observamos que el grupo activo tiene
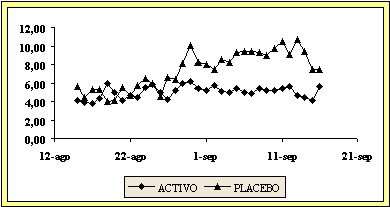
una puntuación muy estable de unos 5 puntos, mientras que el
grupo placebo oscila entre 4 y 10, existiendo diferencias de hasta >40%
entre ambos grupos. La estadística comparativa del escore global de síntomas
demuestra que existen diferencias significativas entre ambos grupos (p 0,048).
Activo Placebo
Media 4,83 7,91
Desv. Est 4,36 7,29
Mediana 4,3 5,86
Si además analizamos estadísticamente las diferencias entre ambos grupos considerando los días con puntuación>4 y >10, vemos que también existen diferencias significativas entre ambos, con una p de 0,001 y 0,0039 respectivamente, lo que implica que el grupo placebo se encontraba clínicamente peor que el grupo activo.
En la comparación entre ambos grupos considerando los días con puntuación=0, es decir los días libres de síntomas, no encontramos diferencias estadísticamente significativas (p 0,245), por lo que podemos concluir que en ninguno de los dos grupos hubo más días, de forma global, con ausencia de sintomatología.
2.1-Desde
1-15 Septiembre
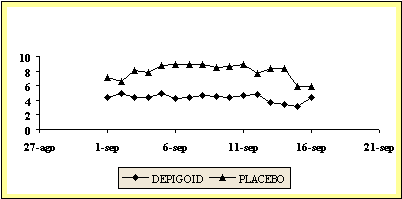
En este periodo
de tiempo vemos que analizando la puntuación
global de síntomas, el grupo activo sigue manteniendo una puntuación de
alrededor de 5, mientras que el grupo placebo tiene 9 puntos; de nuevo existe
una diferencia de >40% entre ambos grupos. Estadísticamente, la comparación
entre ambos grupos demostró que existen diferencias significativas para la
puntuación global de síntomas, días con
puntuación>4, días con puntuación >10 y días con puntuación=0 (días
libres de sintomatología), con una p de 0,049, 0,001, 0,0024 y 0,0029
respectivamente. Esto implica que durante este periodo de tiempo el grupo
activo se encontraba mejor clínicamente
que el grupo placebo y además que tuvieron más días con ausencia de síntomas
que el grupo control.
Activo Placebo
Media 5,38 8,98
Desv. Est 4,93 8,53
Mediana 4,43 6,62
PARÁMETROS CLÍNICOS SECUNDARIOS
1.-Consumo de medicación global
No
se han encontrado diferencias significativas en la toma de medicación en
ninguno de los periodos estudiados.
2.-Test de calidad de vida en
rinitis
Analizando
las diferencias entre T0 y T2, vemos que entre los dos grupos, al final(T2)
existen diferencias significativas entre ambos, que al principio(T0) no
existían. Esto indica que el grupo activo al final se encuentra mucho mejor que
el grupo placebo, mientras que al inicio ambos grupos se encontraban igual. Si
comparamos ahora los valores del inicio y del final en cada grupo por separado,
vemos que no existen diferencias significativas en la calidad de vida en el
grupo placebo, mientras que sí las hay en el grupo activo. Podemos concluir que
el grupo activo se encuentra mejor al final del estudio que al principio y que
el grupo placebo no experimenta cambios en este periodo.
Intergrupo: Inicio Final
p 0,6669 0,0481
Intragrupo: Activo Control
p 0,0011 0,9007
RESULTADOS
DE LA INMUNOTERAPIA
1.-Monitorización de la
inmunoterapia.
Los 41 pacientes
se adecuaron a la normativa general de administración del tratamiento,
alcanzando todos ellos la dosis máxima. En total se administraron 697 dosis,
205 en la iniciación y 492 en el mantenimiento. Cada paciente recibió en la
iniciación 5 inyecciones y 12 en el mantenimiento. La duración total del
tratamiento fue de unas 49 semanas, realizando la iniciación en 2 días (1ª
semana) y el mantenimiento a lo largo de las 48 restantes.
La dosis
acumulada fue de 925 HEP del extracto nativo en la iniciación y de 6925 HEP en
el mantenimiento.
2.-Tolerancia de la
inmunoterapia.
Las reacciones
que encontramos a lo largo del año de inmunoterapia fueron todas sistémicas.
Estas reacciones fueron un total de 16 en el grupo activo, que representan un
2,29% de las dosis globales, siendo el 3,9% de las dosis de inicio y el 1,62%
de las dosis de mantenimiento. Cabe destacar que las reacciones fueron todas
muy leves y no precisaron de tratamiento alguno.
Tabla 1-Reacciones sistémicas en el grupo
activo (% de pacientes).
Iniciación Mantenimiento
Inmediatas 4 (9,75%) 3 (2,43%)
Tardías 4 (9,75%) 5 (7,31%)
2.1-En la iniciación,
como vemos en la tabla 1 , se presentaron 8 reacciones sistémicas, todas ellas
en pacientes activos; 4 fueron inmediatas en pacientes distintos, encontrando 2
rinitis leves, 1 rinitis moderada y prurito ótico en otro paciente; 4 fueron
tardías, también en pacientes distintos, que se distribuyeron de la siguiente
manera: 3 rinitis leves y prurito ótico.
2.2-A
lo largo del mantenimiento se presentaron:
2.2.1-En el grupo
activo 8 reacciones sistémicas; 3 reacciones fueron inmediatas y ocurrieron
en un mismo paciente; se trataban de rinitis moderadas, lo que llevó a que no
alcanzara la dosis de mantenimiento como los demás, hasta pasada la estación
polínica. Esta misma paciente presentó más tarde un episodio de rinitis leve
tardía y contabilizamos además otras 4 rinitis leves tardías que se presentaron
en dos pacientes diferentes.
2.2.2- En el grupo placebo
en total fueron 4, todas ellas rinitis leves tardías representando el 1,7% de
las dosis y el 15,78% de pacientes.
Contabilizamos
además los nódulos subcutáneos que encontramos; fueron un total de 16, en 8
pacientes diferentes, tanto activos como controles. Todos ellos se produjeron
en el mantenimiento.
DISCUSIÓN
La
IT se ha utilizado en el tratamiento de la enfermedad alérgica desde que fue
introducida por Noon en 1911(1). En la actualidad, es una de las armas
terapéuticas de las que dispone el alergólogo para lograr mejorar o curar, ya
sea parcial o totalmente un proceso alérgico(2). Sin embargo, existen todavía controversias sobre la necesidad de
establecer las dosis adecuadas a
utilizar, el régimen de IT empleado(3) y el extracto alergénico a administrar.
La disponibilidad, en los últimos años, de agentes farmacológicos más potentes
y con menos efectos secundarios, ha condicionado un cambio en el uso de la IT.
Se ha demostrado que la eficacia clínica de los extractos alergénicos
modificados (alergoides) es prácticamente idéntica a la de los preparados no modificados,
aunque su alergenicidad es más de 1000 veces inferior(4). En el caso actual,
con este nuevo extracto despigmentado, polimerizado y adsorbido en AlOH,
existen conclusiones favorables a su eficacia y seguridad para Parietaria j(5) y Olea e(6).
La
inhalación del polen de Salsola kali
es una causa frecuente de manifestaciones alérgicas en Zaragoza(7). En la
literatura no hay estudios que valoren el efecto de una IT específica con
extracto de Salsola k, salvo la Tesis de la Dra. Belén de la Hoz(8), quien
realizó un ensayo prospectivo aleatorio con un grupo activo de 15 pacientes que
fue vacunado con extracto acuoso de Salsola
kali en la iniciación y en el mantenimiento con extracto depot adsorbido en
hidróxido de aluminio, frente a un
grupo control que no fue vacunado. Se obtuvieron diferencias significativas
estadísticamente en la eficacia clínica del tratamiento de la
rinoconjuntivitis, así como en las pruebas cutáneas, provocación nasal y
conjuntival.
En
nuestro trabajo, hemos encontrado una mejoría clínica significativa, buena
tolerancia de la vacuna y además hemos observado un desfase de 10-25 días entre
los picos de polen atmosférico y la máxima sintomatología. Este hecho ya ha
sido observado con anterioridad con otros pólenes, entre los que destacan las
gramíneas, en un estudio multicéntrico aerobiológico de varias ciudades
españolas(9), donde se apuntan varios factores para esta falta de correlación,
entre los que destaca el “efecto priming”.
Con
respecto a la falta de significación estadística en el consumo de medicación
global entre ambos grupos, tenemos que tener en cuenta, no solamente, que
faltan datos todavía por analizar, sino que como ya se ha observado en muchas
ocasiones, los pacientes comienzan la reducción del consumo de fármacos a partir
del 2º año de vacunación.
Quizás
cabría pensar en un principio que hemos presenciado numerosas reacciones
sistémicas en nuestro ensayo, pero como ya hemos comentado todas ellas fueron
muy leves y además encontramos, en el mantenimiento, el mismo % de reacciones
con respecto al número de dosis, en el grupo activo(1,62%), que en el grupo
control(1,7%).
CONCLUSIONES
·
La
utilización de IT en pauta rápida hasta una dosis máxima de 500 HEP con un
extracto de Salsola kali despigmentado
polimerizado y adsorbido en hidróxido de aluminio, durante un año, ha
demostrado:
o
Reducción
significativa en los recuentos globales de síntomas de rinoconjuntivitis y
asma.
o
Aumento
significativo de los días libres de síntomas.
o
Reducción
significativa de días con síntomas intensos.
o
Mejoría
significativa en los cuestonarios de Calidad de Vida de rinoconjuntivitis.
o
Existe
un desfase de aproximadamente 10 días entre los máximos recuentos de polen y
los síntomas más intensos.
·
La
IT con este extracto ha demostrado ser segura:
o
No
hubo reacciones locales.
o
Todas
las reacciones sistémicas fueron leves y no precisaron tratamiento
farmacológico.
o
En
la fase de iniciación todas las reacciones observadas tuvieron lugar en el
grupo activo, mientras que en el mantenimiento ocurrieron de forma similar en
ambos grupos.
BIBLIOGRAFÍA
1.-Noon L. Prophylactic inoculation
against fever. Lancet
1911; 1:1572.
2.-Sociedad Española
de Alergología e Inmunología clínica. Normativa sobre inmunoterapia en enfermedades alérgicas. SANED (2ª edición). 1992; 11.
3.- Malling H-J, ed. Inmunotherapy:
position paper prepared by the Inmunotherapy Subcomittee of the European
Academy of Allergology and Clinical Immunology. Allergy 1988; 43 (suppl 6):
9-13.
4.-Patterson et al. Development and
evaluation of polymerised allergens for inmunotherapy. Int Arch Allergy app
Immunol 1981; 6 (suppl 1): 293-6.
5.-M. Casanovas,
F.J. García-Selles et al. Hipersensibilidad al polen de Parietaria judaica: tolerancia y eficacia de la inmunoterapia con
nuevos extractos químicamente modificados. Allergy 2000; 55 (suppl 63).
6,-F. Guerra et al.
Eficacia y seguridad de la inmunoterapia con vacunas de Olea europaea estandarizadas, despigmentadas y polimerizadas con
glutaraldehído. JACI 200; 105 (1).
7.-J. Pola et al.
Polinosis en el área de Zaragoza. Rev.
Esp. Alergol Inmunol Clin 1998;13 (2): 135-139.
8.-Belén de la Hoz
Caballer. Rinoconjuntivitis y asma por hipersensibilidad al polen de Salsola kali: aspecto
clínico-inmunológicos y valoración de la inmunoterapia. Tesis Doctoral 1995.
9.-J. Subiza et al.
Pólenes alergénicos y polinosis en 12 ciudades españolas. Rev. Esp Alergol Inmunol Clin, 1998; 13 (2):
45-58.