INMUNOTERAPIA
AGRUPADA CON POLEN DE Salsola kali.
S. Monzón, C. Colás, A.
Lezaun, M. Venturini, C. Reichelt , S. Lara.
Hospital Clínico
Universitario. Zaragoza.
INTRODUCCIóN
El polen de la Quenopodiales constituye el 5% de los pólenes anuales en el área de Zaragoza, pero sensibilizan hasta el 42% de los polínicos en nuestra área, ocupando el tercer lugar entre la población polínica de nuestra región por su gran poder sensibilizante.
El año pasado presentamos los resultados del ensayo doble ciego
controlado con placebo realizado con 41 pacientes a quienes se les administró
una pauta cluster de S. Kali durante
2000-2001. Los 19 pacientes que
habían pertenecido al grupo placebo, fueron vacunados al año siguiente
(2001-2002) con otra pauta agrupada diferente y un extracto depot de S. Kali. Este año presentamos los resultados que tenemos a día
de hoy comparando estos tres grupos.
OBJETIVOS
El objetivo ha
sido valorar tanto la eficacia como la
seguridad de la inmunoterapia. Para apoyar la eficacia de la inmunoterapia,
se ha tenido en cuenta tanto la sintomatología clínica, que es la variable
principal del estudio, como los parámetros clínicos secundarios:
·
Variable clínica principal: Sintomatología Clínica
o
Recuento de puntuación global de síntomas
·
Parámetros Clínicos Secundarios:
o
Recuento de puntuación de consumo de medicación
o
Cuestionario de calidad de vida en rinitis
o
Escala visual
o
P.Cutáneas
o
Provocación nasal
o
Pruebas in vitro
–Ig E total.
–Ig E específica.
–Ig G específica, Ig
G1 e Ig G4 alergeno específicas.
Para apoyar la seguridad de la inmunoterapia,
aportaremos los datos de la monitorización y tolerancia de la misma.
MATERIAL
Y MéTODOS
1.-Criterios de inclusión y exclusión:
1.1-Criterios de inclusión:
-Historia clínica
muy sugestiva de rinitis y/o asma debido a sensibilización frente al polen de Salsola kali.
-Edad comprendida
entre los 18 años cumplidos y los 55 años cumplidos.
-Sintomatología
concordante de rinitis y/o asma estacional en la época de polinización de las
chenopodiáceas.
-Test cutáneos positivos
a Salsola kali: la pápula que
producirá el test cutáneo por medio de la técnica del prick-test debe ser igual o superior a 6 mm de
diámetro.
-Deben ser capaces de
cumplir el régimen de dosificación y de dar el consentimiento informado.
1.2-Criterios de exclusión:
-Pacientes sensibilizados a
otros pólenes distintos de la familia de las Chenopodiáceas y/o hongos y/o
ácaros.
-No podrán incluirse los
pacientes que hayan recibido previamente inmunoterapia en los últimos cuatro
años. Tampoco podrán incluirse los pacientes en los que la inmunoterapia pueda
ser objeto de contraindicación general absoluta.
2.-Criterios de retirada:
Los pacientes podrán ser
retirados del estudio en cualquier momento, si:
-El paciente decide
retirarse del estudio
-El investigador decide
retirar al paciente del estudio:
por empeoramiento del estado del
paciente, aparición de efectos adversos graves, enfemedad intercurrente, o mala
colaboración del paciente.
3.-Cronograma del estudio
A continuación os presento los cronogramas de
los estudios realizados tanto con alergoide como con extracto depot de S. Kali (Figuras 1 y 2):
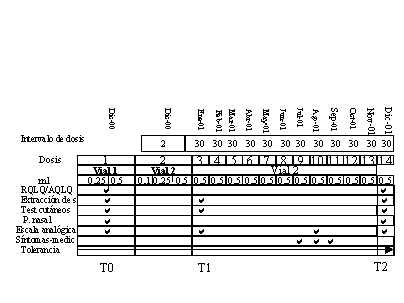
Figura 1.-Cronograma del
grupo vacunado con Alergoide (2000-2001)
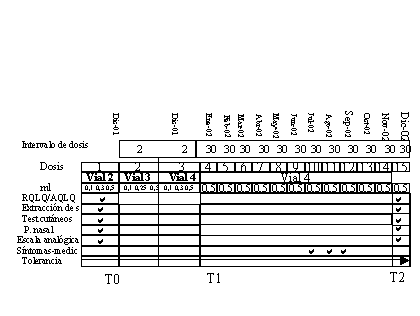
Figura 2.-Cronograma del
grupo vacunado con Depot (2001-2002)
4.-Cartilla de síntomas
La recogida de síntomas se llevó a cabo mediante unas cartillas donde,
en una primera página ponían sus iniciales, el número que se les había asignado
y la semana en la que se encontraban. En la segunda página iban calificando
cada día por la mañana y por la noche la intensidad de sus síntomas nasales,
oculares y bronquiales. La puntuación variaba desde el cero cuando no habían
experimentado ningún síntoma hasta el 3 cuando ese síntoma había llegado a
interferir en su actividad diaria; pasando por el 1 cuando el síntoma había
estado presente sin molestar y el 2 cuando había llegado a molestar sin
interferir en la vida diaria. El rango de puntuación obtenido variaba desde el
0 hasta 54 puntos.
5.-Consumo de medicación
La medicación
sintomática fue prescrita de modo gradual según criterio del médico a demanda
del paciente. De forma paralela a la recogida de síntomas el paciente fue
rellenando en su cartilla cada día la medicación consumida y posteriormente se
realizó un score detallado de dicha medicación asignando a cada escalón
terapeútico una puntuación determinada. Así por ejemplo, la toma de un
comprimido de antihistamínico fue calificadada como rinitis de primer nivel y
se le asignó un uno en nuestra escala. A la asociación de antihistamínico más
vasoconstrictor le correspondía la puntuación de dos puntos y así sucesivamente
con los distintos fármacos que aconsejábamos para el tratamiento de la rinitis,
conjuntivitis y el asma, que por supuesto eran los mismos fármacos para todos
los pacientes.
6.-Pauta de inmunoterapia
6.1-Alergoide
(2000-2001):
La dosis inicial
fue de 0,25 y 0,5ml de un vial de 100 HEPL/ml del extracto nativo sin modificar
en un día y 0,1, 0,25 y 0,5 de un vial de 1000 HEPL/ml del extracto
nativo sin modificar en otro día. La pauta de iniciación se realizó en dos días
alternos de una misma semana y la de mantenimiento fue de 0,5 ml del vial de
máxima concentración en dosis mensuales (500 HEPL del extracto nativo), durante
12 meses.
6.2-Depot
(2001-2002):
La dosis inicial fue de 0,1, 0,3 y 0,5ml de un vial de 1 HEPL/ml
en un día; 0,1, 0,3 y 0,5 de un vial de
10 HEPL/ml y 0,1, 0,3 y 0,5 ml de un vial de 100 HEPL/ml en otro día. La
pauta de iniciación se realizó en tres días alternos de
una misma semana y la de mantenimiento fue de 0,5 ml del vial de máxima
concentración en dosis mensuales (50 HEP), durante 12
meses.
CARACTERíSTICAS
DE LOS PACIENTES
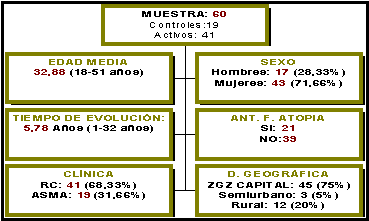
Las características de los
pacientes quedan recogidas en la siguiente tabla:
SINTOMATOLOGíA CLíNICA
1.-Recuento de puntuación de síntomas de forma global:
1.1- GrupoAlergoide:
Analizando la puntuación global de síntomas,
observamos que el grupo vacunado con un extracto alergoide de S. Kali tiene una puntuación muy estable
de unos 5 puntos, mientras que el grupo placebo oscila entre 4 y 10, existiendo
diferencias de hasta >40% entre ambos grupos, sobre todo a partir del pico
de polinización, que señalamos con una flecha. La estadística comparativa del
escore global de síntomas demuestra que existen diferencias significativas
entre ambos grupos (p <0,01)
(Gráfica 1).
Gráfica 1.- Comparación
síntomas globales entre grupo placebo y vacunado con alergoide
1.2- Grupo Depot :
Analizando la puntuación global de síntomas,
observamos que el grupo vacunado con un extracto depot de S. Kali tiene una puntuación muy estable de unos 5 puntos, mientras
que el año anterior, oscilaba entre 4 y 10, existiendo diferencias de hasta
>40% entre ambos, sobre todo a partir del pico de polinización, que
señalamos con una flecha. La estadística comparativa del escore global de
síntomas demuestra que existen diferencias significativas entre ambos años (p <0,001) (Gráfica 2).
![]()
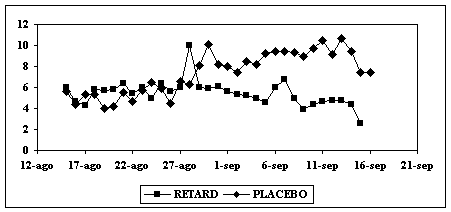
Gráfica 2.- Comparación
síntomas globales antes y después de la inmunoterapia en el grupo vacunado con
depot.
2.-Consumo de medicación.
2.1-Grupo
Alergoide.
En
cuanto al análisis estadístico del consumo de medicación vemos que existen
diferencias significativas entre ambos grupos(p<0,001), lo que implica que
(Gráfica 3):
•Grupo Placebo:
Hasta Septiembre no necesita casi tratamiento; a partir de entonces el escore
aumenta desde 0,3 hasta 1,3.
•Grupo Alergoide: El
consumo de medicación es prácticamente a lo largo del periodo de polinización
de S. Kali alrededor de 0,7 en el escore.
![]()
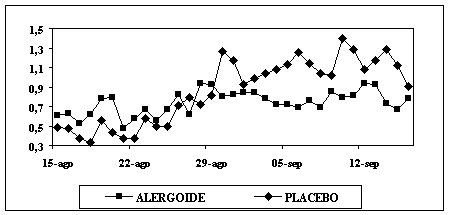
Gráfica3-Comparación del consumo de medicación entre
Alergoide y Placebo.
2.2-Grupo depot.
Este verano observamos que hasta principios de Agosto el grupo Retard consume más medicación que el año anterior cuando no llevaba IT, lo que nos hace suponer que esta estación polínica ha tenido más concentración diaria de polen que el año previo. Posteriormente a partir de septiembre se redujo el consumo de medicación en el grupo Retard. No se han demostrado diferencias significativas entre ambos años para el consumo de medicación(Gráfica 4).
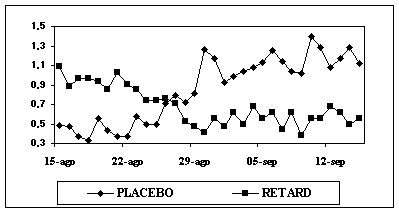
Gráfica
4-Comparación del consumo de medicación en el grupo depot, antes y después de
la IT
RESULTADOS DE LA INMUNOTERAPIA
1.-Monitorización de la inmunoterapia en el grupo Alergoide.
Los 41 pacientes
se adecuaron a la normativa general de administración del tratamiento,
alcanzando todos ellos la dosis máxima. En total se administraron 697 dosis,
205 en la iniciación y 492 en el mantenimiento. Cada paciente recibió en la
iniciación 5 inyecciones y 12 en el mantenimiento. La duración total del
tratamiento fue de unas 49 semanas, realizando la iniciación en 2 días (1ª semana)
y el mantenimiento a lo largo de las 48 restantes.
La dosis
acumulada fue de 925 HEP del extracto nativo en la iniciación y de 6925 HEP en
el mantenimiento.
2.- Monitorización de la inmunoterapia en el grupo Depot
Todos los pacientes
se adecuaron a la normativa general de admón.
del tto. Fueron sometidos a IT
un total de 19 pacientes. Se administraron un total de 399 dosis, de las que:
Iniciación-171 (42,86%)
Mantenimiento-228 (57,14%)
-Cada paciente recibió en la iniciación 9 inyecciones y en el mantenimiento 12 .La duración del tto. fue de 1 año (Dic 01-Dic 02), es decir de unas 49 semanas, que se repartieron: iniciación 1 semana y mantenimiento 48 semanas. Todos los pacientes alcanzaron la dosis máxima administrada (0,5 ml del vial 2).La dosis acumulada total fue de: iniciación 99,9 HEP y mantenimiento 699,9 HEP
3.-Tolerancia de la inmunoterapia.
3.1-Grupo
Alergoide
Las reacciones que encontramos a lo largo del
año de inmunoterapia fueron todas sistémicas. Estas reacciones fueron un total de
16 en el grupo activo, que representan un 2,29% de las dosis globales, siendo
el 3,9% de las dosis de inicio y el 1,62% de las dosis de mantenimiento. Cabe
destacar que las reacciones fueron todas muy leves y no precisaron de
tratamiento alguno.
Tabla 1-Reacciones
sistémicas en el grupo activo (% de pacientes).
Iniciación Mantenimiento
Inmediatas
4 (9,75%) 3 (2,43%)
Tardías
4 (9,75%) 5 (7,31%)
3.1.1-En
la iniciación, como vemos en la tabla 1 , se presentaron 8 reacciones
sistémicas, todas ellas en pacientes activos; 4 fueron inmediatas en pacientes
distintos, encontrando 2 rinitis leves, 1 rinitis moderada y prurito ótico en
otro paciente; 4 fueron tardías, también en pacientes distintos, que se
distribuyeron de la siguiente manera: 3 rinitis leves y prurito ótico.
3.1.2-A
lo largo del mantenimiento se presentaron:
-En
el grupo activo 8 reacciones sistémicas; 3 reacciones fueron inmediatas
y ocurrieron en un mismo paciente; se trataban de rinitis moderadas, lo que
llevó a que no alcanzara la dosis de mantenimiento como los demás, hasta pasada
la estación polínica. Esta misma paciente presentó más tarde un episodio de
rinitis leve tardía y contabilizamos además otras 4 rinitis leves tardías que
se presentaron en dos pacientes diferentes.
-
En el grupo placebo en total fueron 4, todas ellas rinitis leves tardías
representando el 1,7% de las dosis y el 15,78% de pacientes.
Contabilizamos
además los nódulos subcutáneos que encontramos; fueron un total de 16, en 8
pacientes diferentes, tanto activos como controles. Todos ellos se produjeron
en el mantenimiento.
3.2-Grupo Depot
Las reacciones que encontramos a lo largo del
año de inmunoterapia fueron un total de 3, que representan un 0,75% de las dosis globales, siendo el 1,17%
de las dosis de inicio y el 0,44% de las dosis de mantenimiento.
Tabla 2-Reacciones
sistémicas en el grupo depot (% de pacientes).
Iniciación
Mantenimiento
Inmediatas
1 (8,33%) 1 (8,33%)
Tardías
1 (8,33%) 0
3.2.1-En
la iniciación, como vemos en la tabla 2 , se presentaron 2 reacciones,
una local inmediata de >5cm,en un paciente con dosis 0,5/4, que no volvió a
repetirse en las siguientes dosis y una rinitis leve, con dosis 0,5/2 que no
precisó de ningún tratamiento.
3.2.2-A
lo largo del mantenimiento se presentó una rinitis leve inmediata, que
tampoco precisó de tratamiento.
No contabilizamos ningún nódulo s.c con este
tipo de extracto.
CONCLUSIONES
•A
lo largo de estos dos años con dos pautas cluster y dos extractos de S. Kali, hemos objetivado:
–Reducción en los
recuentos globales de síntomas en pacientes vacunados tanto con alergoide como
con el extracto retard, existiendo diferencias significativas entre antes y después de la administración
de IT en ambos grupos.
–Reducción en el
consumo de medicación en pacientes vacunados tanto con alergoide como con el
extracto retard, existiendo diferencias significativas entre antes y después de la administración
de IT en el grupo con alergoide, pero no en el grupo retard.
BIBLIOGRAFíA
·
J. Pola et al. Polinosis en el área de
Zaragoza. Rev. Esp. Alergol Inmunol Clin 1998;13 (2): 135-139.
·
Noon L. Prophylactic inoculation against fever. Lancet 1911; 1:1572.
·
Sociedad Española de Alergología e
Inmunología clínica. Normativa sobre
inmunoterapia en enfermedades alérgicas. SANED (2ª edición).
1992; 11.
·
Malling H-J, ed. Inmunotherapy: position paper
prepared by the Inmunotherapy Subcomittee of the European Academy of
Allergology and Clinical Immunology. Allergy 1988; 43 (suppl 6): 9-13.
·
Patterson et al. Development and evaluation of
polymerised allergens for inmunotherapy. Int Arch Allergy app Immunol 1981; 6
(suppl 1): 293-6.
·
M. Casanovas, F.J. García-Selles et al.
Hipersensibilidad al polen de Parietaria
judaica: tolerancia y eficacia de la inmunoterapia con nuevos extractos
químicamente modificados. Allergy 2000; 55 (suppl 63).
·
F. Guerra et al. Eficacia y seguridad de la
inmunoterapia con vacunas de Olea
europaea estandarizadas, despigmentadas y polimerizadas con glutaraldehído.
JACI 200; 105 (1).
·
Belén de la Hoz Caballer. Rinoconjuntivitis y
asma por hipersensibilidad al polen de Salsola
kali: aspecto clínico-inmunológicos y valoración de la inmunoterapia. Tesis
Doctoral 1995.
·
Subiza et al. Pólenes alergénicos y polinosis
en 12 ciudades españolas. Rev. Esp Alergol Inmunol Clin, 1998; 13 (2):
45-58.